
这可能是近年来对医疗行业影响最大的一份文件。
长期以来,细胞治疗、基因编辑、干细胞等前沿生物医学技术在国内处于"监管真空"地带——技术已经跑通了,但规则没跟上。医院想做,但不知道能不能做、怎么做;企业想投,但担心政策风险;患者想用,但找不到正规渠道。
2025年9月28日,国务院签署第818号令——《生物医学新技术临床研究和临床转化应用管理条例》,2026年5月1日起正式施行。这是中国生物医学新技术监管史上第一次系统性地划清"药"和"术"的边界。
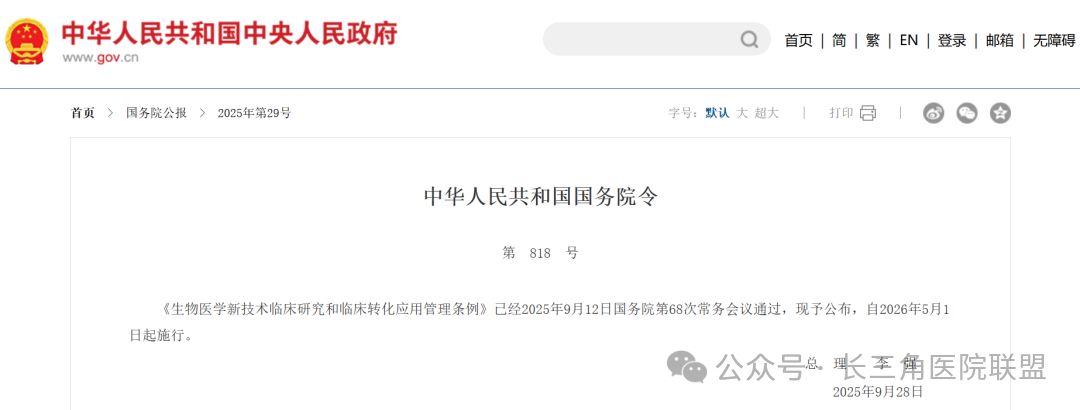
2026年1月16日,国务院再签第828号令——《中华人民共和国药品管理法实施条例》修订版,2026年5月15日起施行。
两道令一起,构成了业内所说的"双轨制":
一句话总结:818管"怎么在医院做",828管"怎么变成药卖"。两条路都通,但不能混走。
对于医院来说,818号令的核心意义在于:首次允许三甲医院作为生物医学新技术的临床研究申办主体,通过备案制快速启动临床研究,并可在符合条件的前提下开展收费转化。这为医院自主开展新技术临床研究打开了新通道。
然而,新政落地并非一帆风顺。审批流程如何操作?备案系统何时开放?收费如何定价?质量如何把控?医生的激励机制怎么建立?这些实际问题尚无细则可依,医院在执行中普遍感到"无从下手"。
正是在此背景下,2026年3月16-18日,中国医药生物技术协会联合上海市生物医药科技产业促进中心、上海生物医药公共技术服务平台、长三角医院联盟等机构组成调研组,赴长三角地区多家大型三甲综合医院开展专题调研,旨在实地了解政策落地中的难点与诉求,为后续推动配套政策制定提供依据,调研苏州大学附属第一医院。
苏大一附院各位领导、专家及多位相关职能部门管理人员对来访调研团表示热烈地欢迎,并详细介绍了苏大一附院的发展历程及在生物及医学新技术的尝试与优势。
苏州大学附属第一医院始创于1883年(清光绪九年),是国家首批三级甲等医院,江苏省卫健委直属的省级医院,江苏省区域医疗中心,江苏省高水平医院、研究型医院和高质量发展省级试点医院。历经140余年发展,现拥有总院区、十梓街院区及转化院区三大医疗区域,开放床位约4000张,年门诊量、手术量位居江苏省前列。医院在血液病学、骨科学、心血管外科等领域具有全国影响力,建有国家临床医学研究中心、国家卫健委重点实验室等多个高能级科研平台。
在生物医学新技术领域,苏大一附院是国内较早开展干细胞临床研究备案的单位之一,医院的"自体骨髓干细胞治疗重症心脏病"项目已于2024年完成国家备案。医院在CAR-T细胞治疗恶性血液肿瘤方面成果显著,曾承担国内首款获批上市的CAR-T产品的临床试验。目前,医院正牵头或参与8项以药品注册为目的的细胞治疗临床研究。此外,在菌群移植、眼科基因治疗、组织工程及脑机接口等方向亦有布局。

苏州大学附属第一医院
调研发现:政策落地仍需配套细则
座谈会上,临床专家普遍反映,818号令的整体方向令人振奋,但在实际执行层面仍面临一些挑战,主要体现在备案流程、质量控制、收费机制、知识产权等方面,有待后续配套文件进一步明确。

调研会现场
专家呼吁:简化流程、放权赋能,激发医疗机构主动性
调研组强调,818号令并非替代原有药品注册路径,而是针对"市场调节失灵"的高成本创新疗法开辟新通道,尤其适用于高度个体化的细胞与基因治疗技术。其核心目标是让真正有效的前沿技术以更低价格、更快速度惠及百姓。
为此,需打破部门壁垒,推动卫健、药监、医保"三医联动",加快制定十四大类生物新技术的临床转化标准。与会专家一致认为,当前中国正处于政策变革窗口期,唯有简化流程、放权赋能、健全标准与激励机制,才能激发医疗机构主动性,实现从"科研强"到"临床强"再到"产业强"的跨越。
邮箱:smia@smia.com.cn
地址:上海市长宁区延安西路1160号 首信银都国际广场1201室

微信公众号